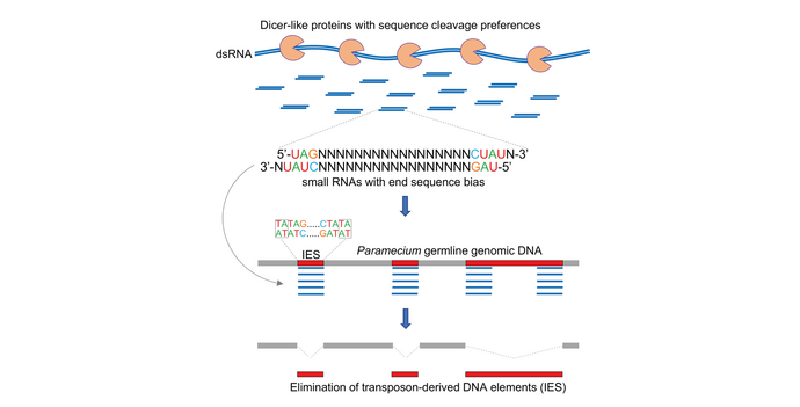
Dicer-Proteine sind im Zellapparat dafür verantwortlich, grosse RNA-Stränge zu zerteilen, um daraus kleinere Moleküle (sRNA) herzustellen. Forschende der Universität Bern haben nun herausgefunden, dass dieser biologische Aktenvernichter nicht einfach wahllos zerhackt, sondern gezielt funktionale Schnipsel produziert. Die so produzierten sRNA-Stücke lösen einen raffinierten zellulären Abwehrmechanismus aus. Zuvor war noch nie ein Dicer-Protein mit ähnlichen Eigenschaften beobachtet worden.
Der Dicer würfelt nicht
In der menschlichen Zelle wie in der menschlichen Gesellschaft: Es dreht sich alles um Information. Gene werden ausgelesen, die Botenmoleküle, sogenannte Messenger RNAs (mRNA), werden verschickt und den Anweisungen entsprechend Proteine zusammengesetzt. Dazu kommen noch eine Unzahl weiterer Botenstoffe – der Zellapparat ist eine grosse Informationsdrehscheibe, ein bis in alle Details fein regulierter Betrieb. Und als wäre das Ganze noch nicht kompliziert genug, zeigte sich in den letzten Jahren immer deutlicher, dass die Regulation zusätzlich noch auf einer höheren Ebene ansetzt. Auch das Informationsmanagement ist hochdynamisch: Informationsmoleküle werden zurückgehalten, verändert, auch kurzerhand wieder geschreddert.
Schnitte werden bewusst angesetzt
Besonders bei Eukaryoten, zu denen auch wir Menschen zählen, spielen diese geschredderten Informationsmoleküle, sogenannte small RNAs (sRNAs) eine entscheidende Rolle bei der Zellentwicklung, der Genexpression und bei der Stabilität des Genoms, das hat die Forschung der letzten Jahre immer deutlicher aufgezeigt. Diese Informationsmoleküle werden von diversen Proteinen hergestellt, dabei gehört «Dicer» zu den am besten untersuchten unter ihnen. Bislang war man eigentlich davon ausgegangen, dass Dicer seine Aufgabe auf einigermassen hemdsärmelige Weise erledigt. Er hackt doppelsträngige RNA in kurze Abschnitte, ohne besonders darauf zu achten, wo die Schnittstellen sind und also auch: Wie die so entstehenden Fragmente aussehen. Doch nun haben Berner Forschende von der Gruppe von Mariusz Nowacki vom Institut für Zellbiologie nachweisen können, dass es zumindest in Pantoffeltierchen Dicer-artige Enzyme gibt, die sehr viel spezifischer schnipseln. Das Ergebnis könnte neue Einblicke in die Regulation der Zellkommunikation ermöglichen und zeigt dazu interessante Möglichkeiten für das gerade erst sich etablierende Feld des Protein-Engineering auf.
Die Forschungsgruppe, die Teil des Nationalen Forschungsprogramms «RNA and disease» ist, hat unlängst im renommierten Fachmagazin Cell von ihrer Entdeckung berichtet. Cristina Hoehener, Iris Hug, und Mariusz Nowacki konnten aufzeigen, dass die von ihnen gefundenen Dicer-Enzyme strikte Grössen- und ausgeprägte Sequenzvorlieben haben. Diese Vorlieben führen dazu, dass sRNAs produziert werden, die perfekt zu den entsprechenden DNA-Abschnitten passen und sich an diesen anlagern. Die Forschenden gehen deshalb davon aus, dass diese Enzyme und ihre RNA-Produkte Teil eines noch nie beschriebenen Abwehrmechanismus sind.
sRNA-Schnipsel reparieren DNA
Ihre Theorie: Die neu entdeckten Dicer-Proteine sorgen für die Eliminierung von ungewollten Erbgut-Abschnitten, ausgelöst durch die präzise Anlagerung der sRNA an den richtigen Stellen der DNA. Es handle sich dabei vermutlich um einen Abwehrmechanismus gegen transposonähnliche Elemente, sagt Cristina Höhener, die das Forschungsprojekt geleitet hat. Transposons sind in die DNA eingeschleuste Fremdcodes, mit der besonderen Eigenschaft, dass sie im Erbgut von einer Stelle zur anderen springen und so alle möglichen unguten genetischen Programme auslösen können. Solche Abschnitte sollte ein Organismus daher möglichst rasch und effektiv wieder loswerden, wobei eben die spezielle Dicer-Häckseltechnik helfen könnte.
Für die Forschenden besonders interessant ist dabei der Grad der Präzision. Es gibt Schneidenzyme, die weit spezifischer als Dicer zu Werke gehen und nur an ganz bestimmten Stellen zum Schnitt ansetzen. Eine allzu strikte Präferenz wäre bei Dicer allerdings nicht zweckdienlich: Für die effektive DNA-Reparatur ist es entscheidend, dass sich relativ viel passende RNA anlagert. Wäre Dicer zu wählerisch, dann würde nicht für alle gefährlichen DNA-Fremdkörper passende Schnipsel produziert werden. Nowacki nennt die neu entdeckte Dicer-Eigenheit eine «relaxed preference», eine entspannte Präferenz. Die in der Summe dann aber doch eine präzise und effektive Reaktion der Zelle auf der DNA-Ebene möglich macht. «Unschärfe ist nicht zwingend eine schlechte Sache in der Biologie», sagt der Zellbiologe. Viele biologische Vorgänge hätten sich im Laufe der Evolution zwischen Präzision und Zufall eingependelt – deshalb können Zellen mit erstaunlich massgeschneiderten Antworten auf ganz verschiedene Umstände reagieren.
Publikationsdetails:
Christina Hoehener, Iris Hug, Mariusz Nowacki (2018): Dicer-like Enzymes with Sequence Cleavage Preferences, Cell, 173(1), 234-247 e7
https://www.sciencedirect.com/science/article/pii/S0092867418301739?via%3Dihub